При взгляде на две прозрачные жидкости или белые аморфные кристаллы, подобные по внешнему виду, непросто понять, какая из них является кислотой, а какая - солью. Однако, существуют некоторые ключевые признаки и определенные методы, помогающие различить эти два химических соединения. Важно знать, на что следует обращать внимание и как применять свои наблюдательные способности.
Уникальные свойства кислот и солей помогают их различить. Кислоты, как правило, обладают кислым вкусом и способны выделять характерную запах. Их реакция с некоторыми металлами может приводить к выделению водорода. Соли, напротив, имеют соленый вкус и не обладают специфическим запахом. Кроме того, они часто образуют характерные кристаллические структуры с уникальными формами и цветами.
Методы определения кислот и солей подразумевают лабораторные исследования. Несмотря на то, что внешний вид может дать некоторую информацию, дополнительные тесты могут быть необходимы для окончательного определения химического состава. Например, кислоты могут быть проверены на реакцию с индикаторами pH, которые изменяют свою окраску в зависимости от кислотности или щелочности раствора. Соли, в свою очередь, могут быть проанализированы на их растворимость в различных растворителях или на наличие определенных ионов через реакции осаждения.
Химический строй кислот и солей: основные различия

Этот раздел посвящен изучению основных различий в химической структуре кислот и солей. Мы рассмотрим особенности атомного строения и взаимодействия, которые позволяют отличить эти две группы химических соединений.
- Атомный состав: Кислоты и соли имеют различные атомные составы. Кислоты обычно состоят из водородного и кислородного атомов, а также других атомов различных элементов. Соли, с другой стороны, состоят из металлических и неметаллических элементов.
- Валентность атомов: Кислоты характеризуются наличием кислотных групп, состоящих из кислородного и других атомов. Эти атомы имеют отрицательную валентность и обычно способствуют образованию ионов в растворе. Соли же имеют положительную и отрицательную валентность, что обуславливает образование ионной решетки.
- Физические свойства: Кислоты обычно обладают кислотными свойствами, такими как кислотный вкус, способность реагировать с металлами и изменять цвет индикаторных растворов. Соли, напротив, обычно обладают соленым вкусом и не обладают кислотными свойствами.
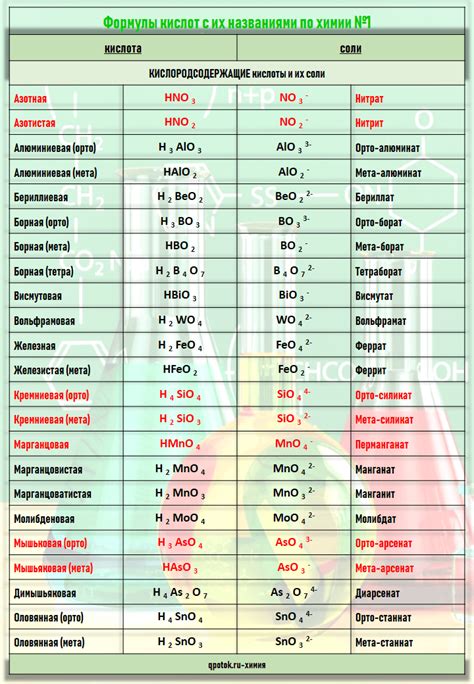
- Формулы: Кислоты обычно обозначаются специфическими химическими формулами, включающими ионные группы. Соли, в свою очередь, также обозначаются химическими формулами, но без наличия ионных групп.
Исследование и понимание основных различий в химической структуре кислот и солей не только поможет различать эти соединения, но и позволит лучше понять их свойства и взаимодействия в различных химических процессах.
Ощущение на ощупь: как отличить физические свойства кислот и солей

При взаимодействии с различными веществами мы обычно ощущаем их свойства через касание. Ощупывая, можно заметить определенные различия в текстуре и состоянии, которые могут помочь отличить кислоту от соли.
Физические свойства кислот:
Когда мы прикасаемся к кислоте, она часто вызывает ощущение жидкости или липкости. Кислоты могут иметь маслянистую консистенцию или быть слегка густыми. При касании кислота может проникать вглубь кожи и вызывать покалывание или ощущение жжения. Кроме того, взаимодействие кислоты с водой может вызывать образование пузырьков или шипение.
Физические свойства солей:
В отличие от кислот, соли обычно ощущаются как твердые и нелипкие вещества. Они могут быть кристаллическими или порошкообразными, с различными формами зерен. При касании, соли обычно нежные и не вызывают дискомфорта на коже. Некоторые соли могут растворяться при намокании, оставляя на ощупь липкость или смолистость.
Зная эти различия физических свойств кислот и солей, можно использовать ощущение на ощупь как хороший способ отличить их друг от друга без необходимости проводить химический анализ.
Вкусовые особенности кислот и солей: как распознать по ощущению во рту

Кислоты могут быть различными по интенсивности вкуса. В меньшей концентрации они могут добавлять продуктам легкую кислинку, в то время как в более высокой концентрации они могут быть острыми и агрессивными для вкусовых рецепторов. Обычно кислоты проявляются в виде лимонной, уксусной или яблочной кислоты, их можно условно назвать «кислыми». Их вкусовые особенности можно ощутить через кислотность и свежесть.
Соли, с другой стороны, обладают свойством подчеркивать и усиливать вкус продуктов. Их характерная соленость может скрывать или, напротив, подчеркивать сладость, горечь или кислотность добавленных ингредиентов. Соль может быть разной по вкусу - морская соль, каменная соль, поваренная соль. Каждая соль даёт свою особенность во вкусе. Легко определить соль вкусом – соль всегда соленая – это и есть ее основная характеристика.
Отличительные черты кислот и солей внешне: внешние признаки
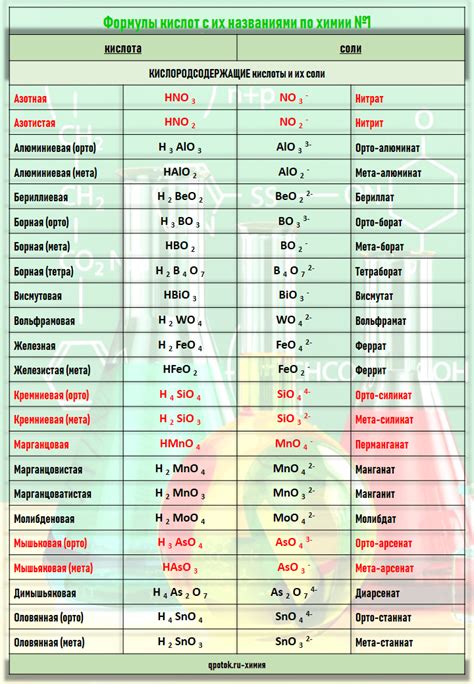
Все вещества, включая кислоты и соли, имеют определенные внешние признаки, которые позволяют их отличать друг от друга. Внешние характеристики могут быть различными и полезными для определения типа вещества без проведения химических экспериментов или анализов.
- Одним из отличительных признаков кислот является их кислотный вкус. Кислотные вещества обладают остро-кислым привкусом, как, например, лимонная кислота или уксусная кислота.
- Еще одним внешним признаком, который помогает различить кислоты, является их способность вызывать жжение и раздражение на коже и слизистых оболочках. Например, серная кислота или соляная кислота могут вызвать ощущение жжения при контакте с кожей.
- Признаки солей, в свою очередь, более разнообразны и могут зависеть от конкретного типа соли. Однако, общим признаком многих солей является их кристаллическая структура. Соли образуют регулярные геометрические кристаллы, которые можно наблюдать под микроскопом.
- Кроме того, соли обычно обладают определенным цветом, который также может помочь в их идентификации. Например, хлорид натрия имеет белый цвет, а хлорид меди - зеленый или синий.
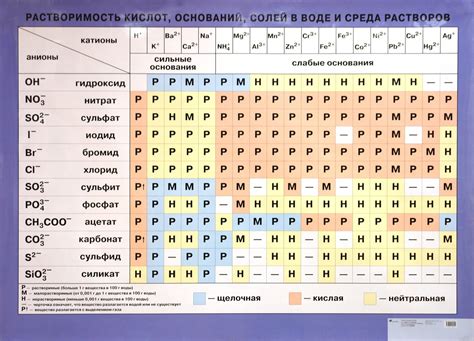
- Еще одним признаком, свойственным солям, является их растворимость в воде. Многие соли легко растворяются в воде, образуя прозрачные растворы, в то время как другие соли могут быть нерастворимыми или образовывать мутную суспензию.
Учитывая эти внешние признаки, можно сделать предположение о том, является ли вещество кислотой или солью. Однако для окончательной идентификации следует использовать более точные методы, такие как химические реакции или спектральный анализ.
Реакция с щелочными веществами: эксперимент для распознавания

Важно отметить, что основания обладают щелочной реакцией и обычно образуют гидроксиды металлов или аммония. Одним из ключевых моментов при проведении данного эксперимента является мысленное моделирование реакции между выбранным веществом и основанием. Наблюдение за характерными признаками реакции поможет определить, к какому классу относится это вещество – кислотам или солям.
При проведении эксперимента следует обратить внимание на изменение физических свойств вещества и окраски раствора при взаимодействии с основаниями. Также важно наблюдать за появлением пузырьков, выделением газа или тепла в результате химической реакции. При соблюдении всех этих аспектов можно с высокой точностью оценить, является ли вещество кислотой или солью.
Использование индикаторов для различения кислот и солей

Реакция индикаторов основана на изменении цвета, которое происходит в результате взаимодействия между индикатором и раствором. Кислоты и соли имеют различные pH-значения, поэтому индикаторы реагируют с ними по-разному. Например, некоторые индикаторы изменяют цвет от кислого к щелочному pH и наоборот. Таким образом, эти изменения в цвете могут указать на тип раствора: кислотный или щелочной.
Для проведения реакции с индикаторами, необходимо добавить небольшое количество индикатора к исследуемому раствору и наблюдать за изменением его цвета. Важно помнить, что каждый индикатор имеет свой конкретный диапазон pH-значений, при котором происходит изменение цвета. Поэтому необходимо выбрать правильный индикатор, соответствующий pH-значению исследуемого раствора.
Реакция с индикаторами является быстрым и удобным способом различения кислот и солей. Она может быть использована как в лабораторных условиях, так и в повседневной жизни, например, для определения pH-значения пищи или воды. Применение индикаторов помогает обнаружить наличие или отсутствие кислотных или щелочных растворов, что может иметь значение в различных химических и биологических процессах.
Современный подход к определению кислот и солей с использованием pH-метра
Одним из основных достоинств использования pH-метра является возможность точного измерения кислотности и щелочности без контакта с раствором. pH-метр представляет собой электронный прибор, состоящий из электродов и измерительного блока. Основным электродом pH-метра является комбинированный электрод, состоящий из стеклянного электрода и электрода сравнения. При измерении pH-метр подключается к раствору и электроны начинают протекать между электродами, создавая разность потенциалов, которая затем измеряется прибором.
Использование pH-метра позволяет определить кислотность или щелочность раствора с высокой точностью и надежностью. Для измерения достаточно поместить электроды pH-метра в раствор и получить значение pH на дисплее прибора. Результаты измерений можно сравнивать с шкалой pH, где значения меньше 7 указывают на кислотность, равные 7 – на нейтральность, а значения больше 7 – на щелочность. Таким образом, используя pH-метр, можно с легкостью определить, является ли раствор кислотным, щелочным или нейтральным.
- Преимущества использования pH-метра в определении кислот и солей
- Точность измерений
- Быстрота и удобство использования
- Не требует контакта с раствором
- Возможность проведения измерений в широком диапазоне pH
- Принцип работы pH-метра и состав электродов
- Комбинированный электрод
- Электрод сравнения
- Интерпретация результатов измерений и определение кислотности/щелочности раствора
- Шкала pH и ее значения
- Примеры кислотных, нейтральных и щелочных растворов
Определение кислот и солей с помощью химических реакций: основные примеры

Одним из примеров такой реакции является образование пузырьков газа при взаимодействии кислоты с металлом. Это явление можно наблюдать, например, при воздействии уксусной кислоты на цинк. При этой реакции происходит выделение водорода в виде пузырьков, что говорит о наличии кислоты.
С другой стороны, при взаимодействии соли с кислотой может произойти осадка. Например, соединение натрия и хлорида, образующее поваренную соль, останется без изменений при взаимодействии с кислотой. В то же время, соль меди и нитрат серебра при этой реакции образуют осадок оксида серебра и хлорида меди соответственно. Такое образование осадков говорит о присутствии солей.
Таким образом, химические реакции позволяют отличить кислоты от солей и выявить их основные свойства. С помощью таких примеров можно изучать химию на практике и углубить свои знания о различных веществах и их реакциях.
Биологическая роль кислот и солей: значимость в организме
Одной из основных функций кислот и солей является их участие в обмене веществ. Кислоты, действуя в качестве катализаторов, активируют различные ферменты, ускоряя химические реакции в организме. Соли же, в свою очередь, выполняют роль электролитов, поддерживая электрическое напряжение между клетками и играя важную роль в проведении нервных импульсов и сокращении мышц.
Кроме того, кислоты и соли являются необходимыми для нормализации кислотно-щелочного баланса в организме. Некоторые кислоты, такие как аминокислоты, являются строительными блоками белка, важного компонента клеток и тканей. Соли же помогают поддерживать оптимальную кислотность внутренней среды, что необходимо для нормальной работы различных систем организма.
Кроме своих основных функций, кислоты и соли также выполняют ряд специализированных ролей. Например, некоторые кислоты участвуют в процессах свертываемости крови, а соли - в регуляции работы сердечно-сосудистой системы.
- Участие в обмене веществ и катализ химических реакций
- Поддержание кислотно-щелочного баланса
- Строительная функция для клеток и тканей
- Регуляция работы сердечно-сосудистой системы
- Участие в процессах свертываемости крови
Таким образом, кислоты и соли играют незаменимую роль в организме, выполняя разнообразные функции, необходимые для его нормального функционирования. Понимание их значения важно для поддержания здоровья и обеспечения правильной работы всех систем организма.
Различие между кислотами и солями в повседневной жизни: полезное знание для каждого

Как мы можем использовать наше знание о различии между кислотами и солями в повседневной жизни? Этот раздел поможет вам осознать, как эти вещества взаимодействуют с окружающей средой и как их использование может оказать положительное влияние на нашу жизнь.
- Выбор безопасных моющих средств
- Правильное хранение пищевых продуктов
- Дезинфекция и очистка
- Особые свойства кислот и солей в медицине
- Экологические применения
Одним из способов применения наших знаний о различии между кислотами и солями в повседневной жизни является выбор безопасных моющих средств для нашего дома. Мы можем обратить внимание на метки на упаковке и избегать продуктов, содержащих агрессивные кислоты, которые могут нанести вред нашим рукам и поверхностям. Вместо этого мы можем выбирать средства, содержащие соли, которые эффективно справляются с загрязнениями и одновременно менее опасны для нашего здоровья.
Кроме того, знание о различии между кислотами и солями поможет нам правильно хранить пищевые продукты. Мы можем избегать использования кислотных консервантов, которые могут изменить вкус и структуру пищи, и предпочитать соли, которые сохраняют свежесть и приятный вкус продуктов насыщенными.
В повседневной жизни мы также можем использовать наше знание о различии между кислотами и солями для дезинфекции и очистки. Например, мы можем использовать кислоты для устранения вредных бактерий и грибков в наших ванных комнатах и кухнях. Однако, когда дело доходит до чистки поверхностей, которые постоянно контактируют с кожей или пищей, мы можем предпочитать использование безопасных солей, которые будут эффективно очищать без негативного влияния на окружающую среду и наше здоровье.
Другой областью, где различие между кислотами и солями применяется в повседневной жизни, является медицина. Кислоты и соли играют важную роль в процессе обработки ран, контроле уровня pH и балансе электролитов в нашем организме. Поэтому, понимая их свойства и воздействие, мы можем правильно использовать рекомендуемые лекарственные препараты и средства для поддержания нашего здоровья.
Наконец, наше знание о различии между кислотами и солями может быть полезным в экологической сфере. Мы можем использовать соли для биоразлагаемых удобрений, которые минимизируют негативное воздействие на окружающую среду, в отличие от кислотных удобрений, которые могут загрязнять почву и воду. Кроме того, мы можем применять соли для очистки и фильтрации воды, что помогает бороться с проблемой загрязнения водоемов и обеспечивает более безопасное питьевое водоснабжение.
Вопрос-ответ

Какие методы можно использовать для определения кислоты и соли?
Для определения кислоты и соли можно использовать несколько методов. Один из них - метод кислотно-основного титрования, при котором при помощи специальных реагентов измеряется количество кислоты или соли в растворе. Еще один способ - использование индикаторов, которые меняют цвет в зависимости от кислотности или щелочности раствора. Также можно провести электрохимический анализ, основанный на измерении электрического потенциала раствора. Важно подобрать подходящий метод в зависимости от конкретного вещества и условий проведения анализа.
Какие признаки позволяют отличить кислоту от соли?
Одним из основных признаков, позволяющих отличить кислоту от соли, является вкус. Кислоты имеют кислый вкус, в то время как соли обладают соленым вкусом. Кроме того, кислоты способны при взаимодействии с металлами выделять газы, например, водород. Соли же не обладают таким свойством. Также, при растворении в воде кислоты могут образовывать кислотные растворы, увеличивая концентрацию ионов водорода, в то время как соли дают нейтральные растворы.
Как можно определить кислотность или щелочность раствора?
Определить кислотность или щелочность раствора можно с помощью индикаторов. Индикаторы - вещества, меняющие цвет в зависимости от кислотности или щелочности раствора. Например, универсальный индикатор меняет цвет от красного (кислотная среда) до фиолетового (щелочная среда) в зависимости от pH раствора. Также можно использовать специфические индикаторы, которые меняют цвет только в определенном pH-диапазоне.
Существует ли универсальный метод для определения кислот и солей?
Универсального метода для определения всех возможных кислот и солей не существует. Каждое вещество имеет свои характерные свойства, поэтому для определения кислоты или соли необходимо использовать различные методы. Однако, некоторые общие подходы, такие как кислотно-основное титрование или использование индикаторов, могут быть применены при анализе большинства кислот и солей.
Какие признаки помогут отличить кислоту от соли?
Ответ: У кислот и солей есть несколько характерных признаков, которые помогут отличить их друг от друга. Во-первых, кислоты обладают кислым вкусом, в то время как соли - вкусом соли. Во-вторых, кислоты могут вызывать жжение на коже или раздражение слизистых оболочек, в то время как соли не обладают подобными свойствами. Также, кислоты могут иметь характерный запах, который отсутствует у солей. Помимо этого, можно провести некоторые химические эксперименты, такие как использование индикаторных бумажек, чтобы определить кислотность или щелочность вещества.
Какие методы можно использовать для определения кислоты или соли?
Ответ: Для определения кислоты или соли можно использовать несколько методов. Один из таких методов - использование индикаторных бумажек. Их можно погрузить в раствор вещества и по цветовой реакции определить, является ли оно кислотой, щелочью или нейтральным. Также можно провести нейтрализационную реакцию, добавив кислоту или соль к раствору, содержащему известную концентрацию щелочи или кислоты. Если раствор станет нейтральным, значит, реагент является щелочью или кислотой соответственно. Помимо этого, можно использовать химические реактивы, специальные приборы или кондуктометр для определения кислотности или щелочности вещества.