Каждый атом - удивительная капля жизни в бесконечном космическом океане. И в этом океане, как в невидимом мире таинственных сил, расположены энергетические уровни - невидимые ступени, на которых совершаются их магические танцы. Внешний энергетический уровень, словно граница между видимым и невидимым, излучает непостижимую силу и влияет на весь атому исполнение.
Когда мы проникаем в это микространство, нас окружает незримая аура энергии и возникает необычное созерцание удивительного балета, в котором атомы играют роли танцоров и зрителей одновременно. Здесь, на внешнем энергетическом уровне, мы находимся на границе энергетического состояния, исходящего от других атомов, и нашей собственной энергии.
Особенность внешнего энергетического уровня заключается в его природе: он находится в постоянном потоке энергии, пронизывающей собой окружающие атомы. Это место, где происходят химические реакции, где рождаются новые связи и изменяется судьба атомов. Влияние внешнего энергетического уровня на жизнь атома нельзя недооценивать, ведь именно здесь зачинаются все последующие изменения на более глубоких ступенях его существования.
Механизм формирования внешнего энергетического уровня в атоме

Рассмотрим процесс, благодаря которому в атоме формируется внешний энергетический уровень, обеспечивающий устойчивость и участие в химических реакциях. Понимание механизма образования этого уровня поможет нам лучше осознать важность его роли во взаимодействии атомов.
- Квантовая механика. Появление внешнего энергетического уровня обусловлено квантовыми свойствами атома, описываемыми квантовой механикой. В соответствии с этой теорией, энергия атома квантуется, то есть принимает определенные дискретные значения.
- Электронные оболочки. В эклектическом представлении, атом состоит из некоторого числа электронов, находящихся на разных энергетических уровнях. Внешний энергетический уровень соответствует наиболее отдаленной от ядра электронной оболочке.
- Процесс заполнения уровней. Внешний энергетический уровень формируется путем последовательного заполнения более близких к ядру энергетических уровней. Электроны, находящиеся на этих уровнях, могут переходить на более отдаленные оболочки, если это обеспечивает более низкую энергию системы.
Таким образом, механизм образования внешнего энергетического уровня в атоме включает квантовую природу энергии, существование электронных оболочек и процесс последовательного заполнения энергетических уровней. Это является важным фактором, определяющим структуру и свойства атомов, а также их взаимодействие в химических реакциях.
Роль электронов и характеристики энергетических уровней
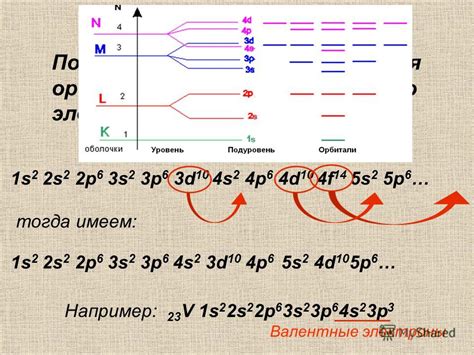
В данном разделе рассмотрим важное влияние электронов на свойства атомов и химические реакции. Также будут представлены основные характеристики энергетических уровней, которые определяют поведение электронов в атоме.
Электроны, находящиеся на различных энергетических уровнях, обладают определенной энергией и могут перемещаться между уровнями. Их распределение определяет химические свойства вещества и способность атомов вступать в химические реакции. Высший энергетический уровень, на котором находятся электроны, играет особую роль при формировании соединений и взаимодействии с другими атомами или молекулами.
| Особенности энергетических уровней: | Влияние на свойства атомов: |
|---|---|
| Энергетический уровень определяется главным квантовым числом и имеет определенную энергию. | Уровень заполненности внешней оболочки электронами влияет на химическую активность атому и возможность образования химических связей. |
| С каждым энергетическим уровнем связана информация о форме орбитали и моменте импульса электрона. | Форма орбитали и момент импульса электрона влияют на магнитные свойства вещества и его взаимодействие с электромагнитным полем. |
| Энергетические уровни представлены в виде энергетической лестницы, где каждый уровень имеет определенный порядковый номер. | Порядковый номер уровня используется для описания электронной конфигурации атомов и может влиять на их позицию в периодической таблице. |
Подробное изучение роли электронов и особенностей энергетических уровней позволяет понять механизмы химических реакций, формирование молекул и свойства вещества в целом.
Роль внешнего энергетического уровня в химических реакциях

Наличие электронов на внешнем энергетическом уровне определяет способность атома образовывать связи с другими атомами. Атомы с неполностью заполненными внешними энергетическими уровнями стремятся образовать стабильные синергетические связи с другими атомами, чтобы достичь устойчивости и нейтрализовать потенциальную энергию. Эти связи, образованные благодаря внешнему энергетическому уровню, называются химическими связями и они играют критическую роль в химических реакциях.
Внешний энергетический уровень атома также определяет его реакционную активность. Чем больше энергии содержит внешний энергетический уровень, тем более активным будет атом в реакции. Атомы с высокоэнергетическими внешними энергетическими уровнями будут более склонны к реакциям и взаимодействиям с другими атомами, чем атомы с низкоэнергетическими внешними энергетическими уровнями.
| Важные понятия | Описание |
|---|---|
| Химическая активность | Способность атомов и молекул взаимодействовать с другими атомами и молекулами |
| Синергетическая связь | Связь, образуемая атомами для достижения стабильности и устойчивости |
| Реакционная активность | Способность атома вступать в химические реакции из-за наличия энергетических резервов |
Взаимодействие с другими атомами и молекулами

В данном разделе мы рассмотрим важную особенность атомов, заключающуюся в их способности взаимодействовать с другими атомами и молекулами. Это взаимодействие играет ключевую роль во многих процессах, определяющих свойства и поведение вещества.
Атомы и молекулы, благодаря своей энергии и структуре, обладают способностью притягивать или отталкивать друг друга. Это взаимодействие основано на различных физических и химических принципах, таких как электростатические силы, ван-дер-ваальсовы силы, обмен электронами и другие.
Взаимодействие атомов и молекул определяет их возможность образовывать химические связи. Химические связи играют фундаментальную роль в создании различных веществ и влияют на их физические и химические свойства. Например, образование ковалентных связей позволяет молекулам обмениваться электронами и образовывать стабильные структуры.
Взаимодействие с другими атомами и молекулами может происходить как в рамках реакций, изменяющих вещества и образующих новые соединения, так и в рамках непосредственного влияния на физические свойства вещества. Например, силы притяжения между атомами и молекулами влияют на температуру плавления и кипения вещества, его плотность, теплопроводность и другие параметры.
Взаимодействие атомов и молекул также может определять их реакционную способность и скорость химических реакций. Некоторые вещества проявляют высокую активность и способность вступать в реакции с другими веществами, в то время как другие могут быть менее реакционноспособными.
Таким образом, взаимодействие атомов и молекул является важной особенностью, которая определяет многие свойства веществ и их поведение в различных условиях. Понимание этого взаимодействия является фундаментальным для развития многих областей науки, включая химию, физику и материаловедение.
Физические изменения материалов под действием различных энергетических уровней

В данном разделе рассмотрим влияние экстернальных энергетических факторов на физические характеристики различных материалов. Под действием разнообразных энергетических уровней можно наблюдать различные физические процессы, которые приводят к изменению структуры и свойств материалов.
Влияние тепловой энергии
Одним из наиболее распространенных энергетических факторов, влияющих на физические свойства материалов, является тепловая энергия. Под действием повышенных температур атомы и молекулы материала начинают вибрировать, что приводит к изменению их расположения и связей. Это может вызывать изменения фазового состояния материала, его плотности, теплопроводности и т.д. Также в процессе охлаждения и кристаллизации материалы могут приобретать новые структуры с определенными свойствами.
Влияние электромагнитных полей
Электромагнитные поля также оказывают заметное влияние на физические свойства материалов. Под действием электромагнитного излучения атомы и молекулы материалов могут изменять свои энергетические состояния, что приводит к изменению их оптических и электрических свойств. Например, в результате воздействия электромагнитного излучения материал может поглощать или отражать свет, изменять электропроводность и магнитные свойства.
Влияние механических воздействий
Наряду с тепловой и электромагнитной энергией, механические воздействия также могут вызывать изменения физических свойств материалов. Под действием силы атомы и молекулы материала могут перемещаться и деформироваться, что приводит к изменению его механических свойств, таких как прочность, упругость и т.д. При этом важную роль играет как величина воздействующей силы, так и скорость и тип деформации.
Таким образом, разнообразные внешние энергетические уровни оказывают значительное влияние на физические свойства материалов, вызывая изменения их структуры и характеристик. Изучение этих эффектов является важной задачей современной материаловедении и позволяет создавать материалы с новыми и улучшенными свойствами для различных областей применения.
Перемещение электрического заряда и его влияние на оптические свойства

В этом разделе мы рассмотрим важный аспект внутренней структуры атома, а именно перемещение электрического заряда, и его влияние на оптические свойства. В атоме, электрический заряд находится на внешнем энергетическом уровне и может передвигаться между атомами вещества. Этот процесс оказывает существенное влияние на оптическое поведение материалов и способствует возникновению различных оптических явлений.
Перенос электрического заряда играет ключевую роль во многих оптических свойствах материалов. Он определяет их прозрачность, поглощение и отражение света. Когда электрический заряд перемещается внутри атома или между атомами, возникают электромагнитные колебания, которые приводят к излучению электромагнитного излучения определенной длины волны.
Оптические свойства материалов также зависят от конкретного местоположения и движения электрического заряда. Например, вещества с большим количеством свободных электронов, таких как металлы, обладают отличными проводящими свойствами и способностью отражать свет. С другой стороны, вещества, в которых электрический заряд плохо перемещается, например, диэлектрики, обладают большей прозрачностью и поглощением света.
Таким образом, понимание процесса переноса электрического заряда и его влияния на оптические свойства материалов является важным для разработки новых оптических материалов, улучшения оптических устройств и понимания различных оптических явлений в природе и технологии.
Химическая активность атома: связь с расположением его внешней энергетической оболочки
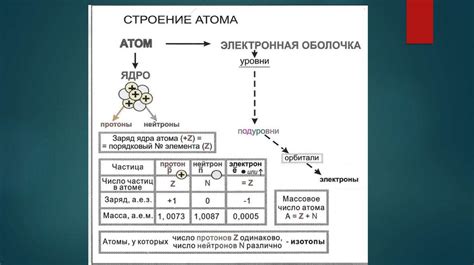
В данном разделе рассматривается важный аспект взаимосвязи между местоположением внешней энергетической оболочки и химической активностью атома. Под химической активностью понимается способность атома участвовать в химических реакциях и образовании химических связей.
Внешняя энергетическая оболочка атома, представленная внешними электронами, играет решающую роль в определении его химических свойств. Поскольку эти электроны находятся на наибольшем удалении от ядра атома, они испытывают наименьшую притягательную силу со стороны положительно заряженного ядра. Это делает их более подвижными и доступными для участия в химических реакциях.
Следует отметить, что расположение атома в периоде таблицы элементов определяет количество электронов в его внешней энергетической оболочке. Например, элементы первого периода имеют только одну электронную оболочку, в то время как элементы второго периода имеют уже две оболочки. Это важно, поскольку количество электронов в внешней оболочке влияет на химическую активность атома. Большее количество электронов на внешнем энергетическом уровне увеличивает возможности атома для формирования ковалентных связей и участия в химических реакциях.
Также следует учесть, что энергия, необходимая для удаления электрона с внешней энергетической оболочки, называемая ионизационной энергией, влияет на степень химической активности атома. Атомы с низкой ионизационной энергией обладают высокой химической активностью, так как легко отдают свои электроны. В то время как атомы с высокой ионизационной энергией обладают низкой химической активностью, поскольку сильно удерживают свои электроны.
Таким образом, местоположение внешней энергетической оболочки атома играет значительную роль в определении его химической активности. Различия в количестве ионизационной энергии на разных энергетических уровнях создают уникальную комбинацию свойств, делающую каждый элемент уникальным в своей способности участвовать в химических реакциях и образовании химических соединений.
Реакционная активность и возможность формирования соединений

Реакционная способность атомов олицетворяет их готовность и способность участвовать в химических реакциях. Чем выше реакционная активность, тем больше вероятность образования соединений. Но важно понимать, что реакционная способность может быть различной в зависимости от местоположения атома внешнем энергетическом уровне.
Наиболее активными являются атомы с неполным электронным оболочкой внешним энергетическим уровне. Они стремятся достичь электронной стабильности путем установления связей с другими атомами. В то время как атомы с полностью заполненной внешней электронной оболочкой обладают меньшей реакционной активностью, так как они уже обеспечены стабильностью и не испытывают потребности в образовании новых связей.
Однако, даже атомы с полностью заполненной внешней оболочкой могут проявлять реакционную способность в некоторых особых случаях. Например, при повышенных температурах или в условиях высокого давления, атомы могут приобретать дополнительную энергию и становиться более активными, формируя новые соединения.
- Реакционная активность атомов зависит от их электронной конфигурации на внешнем энергетическом уровне
- Атомы с неполными внешними электронными оболочками имеют большую реакционную способность, так как они стремятся к электронной стабильности
- Атомы с полностью заполненными внешними электронными оболочками обладают меньшей реакционной активностью, но могут проявлять ее в определенных условиях
Вопрос-ответ

Какое значение имеет местоположение внешнего энергетического уровня атома?
Местоположение внешнего энергетического уровня атома имеет большое значение, так как оно определяет химическую активность атома и его способность вступать в химические реакции. Энергия, связанная с этим уровнем, подразумевает возможность обмена электронами между атомами, что в свою очередь определяет состав и свойства вещества.
Как влияет местоположение внешнего энергетического уровня на структуру атома?
Местоположение внешнего энергетического уровня влияет на структуру атома, так как определяет его электронную конфигурацию. Внешний энергетический уровень содержит в себе валентные электроны, которые, взаимодействуя с другими атомами, образуют химические связи и определяют форму и структуру молекулы.
Какие особенности связаны с местоположением внешнего энергетического уровня?
Особенности, связанные с местоположением внешнего энергетического уровня, включают возможность образования и разрыва химических связей, а также определяют химические свойства атома. Например, атомы с полностью заполненным внешним уровнем обычно являются химически инертными, в то время как атомы с неполностью заполненным внешним уровнем имеют большую склонность к реакциям и образованию химических соединений.
Как внешний энергетический уровень атома связан с его химической активностью?
Внешний энергетический уровень атома является ключевым фактором, определяющим его химическую активность. Если внешний уровень не полностью заполнен или полностью не пуст, то атом будет стремиться достичь более стабильного состояния путем образования химических связей с другими атомами. Это происходит путем обмена или передачи электронов, что в свою очередь приводит к образованию химических соединений и реакций.
Какое влияние оказывает местоположение внешнего энергетического уровня на атом?
Местоположение внешнего энергетического уровня атома имеет существенное влияние на его химические свойства и реактивность. Оно определяет, как атом будет взаимодействовать с другими атомами и молекулами, а также его возможность образовывать химические связи. Например, атомы с полностью заполненными внешними уровнями (например, инертные газы) обладают низкой реактивностью, в то время как атомы с неполностью заполненными внешними уровнями (например, металлы и неметаллы) обычно обладают высокой реактивностью и могут образовывать химические связи с другими атомами, чтобы достичь электронной стабильности.