В природе существуют разные агрегатные состояния веществ, каждое из которых обладает своими уникальными и особыми характеристиками. Одним из таких состояний является газообразное состояние. Газы отличаются от твердых и жидких веществ своими необычными свойствами, которые способствуют их широкому применению в различных сферах нашей жизни.
Газообразные вещества обладают высокими степенями подвижности и диффузии, что позволяет им быстро распространяться и заполнять все имеющееся пространство. Таким образом, они не имеют определенной формы и объема, и это делает их уникальными в сравнении с твердыми и жидкими веществами.
Другой характерной особенностью газов является их компрессибельность – возможность сжатия и расширения под действием давления. Это отличает их от твердых и некоторых жидких веществ, которые обладают значительно меньшей степенью сжимаемости. Благодаря этому свойству газы находят широкое применение в промышленности, где часто требуется изменять объем газового состояния для регулировки процессов.
Основные характеристики газообразных агрегатных состояний материи
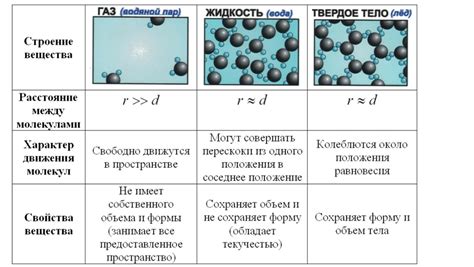
Газообразные вещества внешне прозрачны и обладают низкой плотностью, что связано с большими промежутками между их молекулами или атомами. Они могут существовать при нормальных условиях температуры и давления в атмосфере Земли, либо быть получены из твердых или жидких веществ в ходе нагревания или других процессов.
У газообразных веществ нет определенной формы, они распространяются равномерно и заполняют все доступные им объемы сосуда. Их объем может быть изменен путем изменения давления или температуры. Газы могут сжиматься и расширяться, а также перемещаться в пространстве без ограничений.
Газообразные состояния могут обладать различными физическими и химическими свойствами в зависимости от их молекулярной структуры и межмолекулярных взаимодействий. Эти свойства влияют на их способность растворяться в других веществах, проводить электрический ток, а также на их взаимодействие с окружающей средой и другими веществами.
Изучение газообразных веществ имеет большое значение в различных областях науки и техники, от химии и физики до астрономии и инженерии. Понимание и управление их основными свойствами позволяет разрабатывать новые материалы и технологии, а также предсказывать и объяснять различные физические и химические явления, связанные с газообразными веществами.
Диффузия и распространение газов
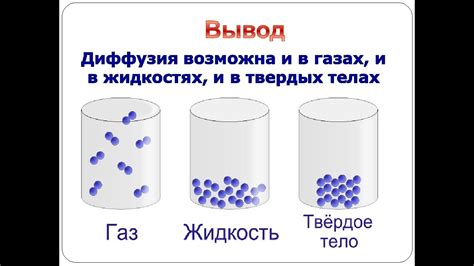
Распространение газов представляет собой одно из фундаментальных свойств газообразных веществ, отличающих их от твердых и жидких состояний. Благодаря этому свойству, газы способны заполнять доступное им пространство и равномерно распределяться, независимо от гравитации и внешних факторов.
Диффузия - явление, описывающее случайное перемешивание молекул различных газов в результате их теплового движения. Это процесс, при котором молекулы воздуха перемещаются из области с более высокой концентрацией в область с более низкой, пока не достигнут равновесия. Диффузия является основной причиной равномерного распределения газов в атмосфере и их смешивания.
Распространение газов - это процесс перемещения газов в пространстве, который может происходить как внутри закрытой системы, так и в открытой среде. Газы могут распространяться под воздействием различных факторов, включая разницу в давлении, температуре или концентрации. Этот процесс имеет большое значение для многих физических, химических и биологических процессов, например, для дыхания организмов или передвижения звука в воздухе.
Таким образом, диффузия и распространение газов представляют важные явления, демонстрирующие уникальные свойства газообразных веществ, включая их способность к равномерному распределению и перемешиванию в пространстве. Эти процессы являются основой для понимания многих физических и химических явлений, а также имеют практическое значение в различных областях науки и техники.
Кинетическая энергия движения молекул газов
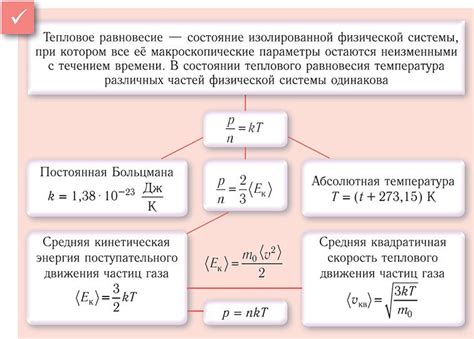
В отличие от твердых и жидких веществ, газы характеризуются высокой подвижностью своих молекул. Благодаря этому, молекулы газа обладают большой кинетической энергией, которая проявляется в их непрерывном случайном движении в пространстве. Эта энергия может быть представлена как энергия теплового движения, обусловленного колебаниями источников тепла.
Стоит отметить, что кинетическая энергия молекул газов является важным фактором, влияющим на другие свойства этих веществ. Например, она определяет давление газов, поскольку при полете молекулы сталкиваются со стенками сосуда, создавая плотность ударов, что приводит к давлению. Также, кинетическая энергия сказывается на температуре, так как более энергичные молекулы газа обладают более высокой температурой.
Таким образом, понимание кинетической энергии молекул газов помогает объяснить особенности их поведения и дает ключевое представление о свойствах этих веществ в состоянии газа.
Установление равновесия в системе газов

Равновесие газов в системе достигается благодаря динамическому взаимодействию между молекулами. Газы постоянно двигаются и сталкиваются между собой, что приводит к обмену энергией и коллизиям. Эти столкновения приводят к изменению скоростей и направлений движения частиц, а также к образованию новых связей и разрывам.
- Равновесие газовых систем может быть установлено при определенных условиях температуры и давления. На эти параметры оказывают влияние внешние факторы, такие как физическое состояние окружающей среды и взаимодействие с другими веществами.
- При достижении равновесия в системе газов, наблюдается стабилизация концентрации каждого компонента и отсутствие изменений в общем объеме.
- Процесс установления равновесия связан с химическими и физическими свойствами газовых веществ, такими как диффузия, сорбция и адсорбция.
- Системы газов могут достичь равновесия как на открытых площадях, так и в закрытых контейнерах. В закрытых системах равновесие может быть установлено при отрицательной обратной связи, когда концентрация одного компонента растет, а другого уменьшается.
Понимание процессов, связанных с установлением равновесия в системах газов, является важным для различных научных и промышленных областей, таких как химия, физика и инженерия. Изучение этого явления позволяет предсказывать поведение газовых смесей и оптимизировать условия для различных процессов и реакций.
Вопрос-ответ

В чем основное отличие свойств газообразных веществ от твердых и жидких?
Главное отличие газообразных веществ от твердых и жидких состоит в их объеме и форме. Газы не имеют определенной формы, они занимают всю доступную им объемную часть сосуда, в котором они находятся. Твердые и жидкие вещества имеют определенную форму и не занимают весь объем сосуда.
Какие свойства газообразных веществ отличают их от твердых и жидких?
Газообразные вещества обладают такими свойствами, как низкая плотность, высокая подвижность, высокая сжимаемость и способность распространяться вплоть до удаленных районов. В отличие от твердых и жидких веществ, газы могут заполнять все имеющееся пространство и растягиваться при изменении объема сосуда, в котором они находятся.
Почему газообразные вещества сжимаемы, в отличие от твердых и жидких?
Газообразные вещества могут быть сжаты из-за больших пространств, которые они занимают в сравнении с их частицами. В газах между частицами существует значительное расстояние, что позволяет им сдавливаться и сжиматься при увеличении давления. В твердых и жидких веществах частицы расположены ближе друг к другу, и поэтому они не обладают высокой сжимаемостью.