Родина частиц - безграничная мирозданная, где молекулы играют главенствующую роль. Прелесть и обаяние этого невидимого мира устроены так, что бесконечное многообразие веществ создает впечатление упорядоченности и хаоса одновременно. От начала времен до современной эпохи исследователи оттачивали свое мастерство, влагая душу и силы в поиск ответа на один из главных вопросов - что образует основную структуру вещей?
Ориентиры на этом пути становятся намного четче с каждым новым открытием молекулярного мира. Набережные научного прогресса увенчаны смелыми гипотезами и страстными исследованиями феноменов, подтверждающими уникальную природу молекулы. Такие одухотворенные рационалисты, как Джон Далтон, Роберт Браун, Авогадро и многие другие, следуя методологическим традициям науки, раскрывают маленькую частичку из большой загадки мира.
Молекула - универсальная строительная единица, представляющая собой почерку подчеркнутого символа, с отчетливо выраженной индивидуальностью и яркой внутренней жизнью. Утонченные танцы, исполняемые молекулами, формируют практически все, что нас окружает - от привычной питьевой воды до самых сложных органических соединений. Волшебное коктейльное сочетание атомов гармонично сплетается в единую сеть макромолекулы, которая открывает перед нами вселенную электронов, прочтенную на поликарбонатной странице с пунктиром и контуром.
Молекулы - основные строительные блоки вещества

Молекулы представляют собой группы атомов, связанных друг с другом определенными химическими связями. Эти связи между атомами определяют структуру и форму молекулы, а также ее свойства. В зависимости от комбинации и расположения атомов, молекулы могут быть разных размеров, форм и массы.
Важно отметить, что молекулы различных веществ могут быть однотипными или разнотипными. Однотипные молекулы состоят из одинаковых атомов или групп атомов. Например, молекулы воды (H2O) состоят из двух атомов водорода и одного атома кислорода, причем подобные молекулы могут существовать только в этом соотношении. В случае разнотипных молекул, в их составе присутствуют разные атомы или группы атомов. Такие молекулы могут быть более сложными и иметь большее разнообразие свойств и химических реакций.
Молекулы играют решающую роль в образовании и превращении веществ. Они обуславливают все процессы в химических реакциях, такие как синтез, разложение, изомеризация. Взаимодействуя друг с другом, молекулы образуют различные химические соединения и структуры, обладающие своими уникальными свойствами и функциями.
История открытия молекулярной структуры вещества

Этот раздел посвящен захватывающей истории, связанной с открытием молекулярной структуры вещества. В течение многих веков ученые исследовали природу мироздания, стремясь понять, из чего состоят вещества и как они взаимодействуют друг с другом.
Интерес к структуре вещества возник еще в древней Греции, когда ученые пытались разобраться в многообразии материи. Но только благодаря развитию научного метода и современной техники удалось достичь прорыва в понимании устройства молекул.
- Античные философы и атомисты предполагали, что все вещество состоит из неделимых частиц – атомов.
- В XIX веке Джон Дальтон сформулировал теорию атомов и молекул, представив материю как набор маленьких частиц, объединенных в определенные структуры.
- Однако только в начале XX века голландский физик Янсма применил рентгеновский метод для изучения кристаллической решетки, доказав, что она состоит из атомов, упорядоченно расположенных в пространстве.
- Одним из самых значительных открытий стал эксперимент Макса фон Лауэ, который в 1912 году показал, что молекулы газов состоят из атомов, а масса каждой молекулы кратна массе атома.
- В 1953 году Джеймс Уотсон и Фрэнсис Крик предложили структурную модель ДНК в виде двойной спирали, открытие которой стало революцией в молекулярной биологии.
История открытия молекулярной структуры вещества ярко демонстрирует, насколько научные открытия и исследования меняют наше представление о мире. Результаты этих исследований оказывают глубокое влияние на многие области науки, от химии и физики до биологии и медицины, и помогают нам лучше понять и использовать свойства веществ для достижения различных целей.
Типы молекул, распространенные в природе
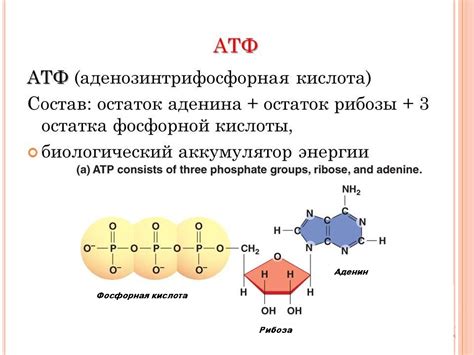
Возможно, мало кого оставит равнодушными факты о разнообразии молекул, встречающихся в природе. Каждая молекула, будь то органическая или неорганическая, обладает своей уникальной структурой и функцией, что непременно влияет на свойства веществ, в которых они содержатся.
Исследование различных типов молекул имеет глубокое практическое значение. Например, понимание органических молекул на основе углерода помогает в разработке новых лекарственных препаратов и синтезе полимеров, а изучение неорганических молекул позволяет понять принципы химических реакций в природных системах и разработать новые материалы с определенными свойствами.
| Тип молекулы | Примеры |
|---|---|
| Углеводороды | метан, этан, пропан |
| Аминокислоты | глицин, лейцин, аспартат |
| Нуклеиновые кислоты | ДНК, РНК |
| Липиды | холестерол, триглицериды |
| Полисахариды | целлюлоза, крахмал |
| Пептиды | инсулин, глюкагон |
Кроме перечисленных типов, существует множество других молекул, которые играют важную роль в различных процессах жизнедеятельности организмов и природных явлениях. Например, вода - простейшая молекула, которая является неотъемлемым компонентом всех живых организмов. Важно отметить, что каждый тип молекулы имеет свою уникальную структуру, которая определяет ее свойства и функции.
Молекулярные соединения: ключевая составляющая химических реакций

В мире химии молекулы играют важную роль, являясь основными строительными блоками веществ. Образуя молекулярные соединения, они определяют физические и химические свойства вещества и влияют на его поведение в различных условиях. Молекулярные соединения могут быть простыми или сложными, и они обладают уникальными свойствами, которые определяют их роль в химии.
Важно отметить, что молекулярные соединения формируются путем соединения атомов различных элементов. Эти атомы могут образовывать различные типы связей, включая ковалентные, ионные или металлические. Именно комбинация атомов и типы связей между ними определяют структуру и свойства молекулы. Кроме того, молекулы могут быть одноатомными или многолучевыми, что также влияет на их реакционную способность и стабильность.
Молекулярные соединения широко использованы в химической промышленности, лабораторных исследованиях и повседневной жизни. Они используются для создания новых материалов, лекарств, пищевых добавок и многого другого. Более того, молекулярные соединения играют ключевую роль в химических реакциях. При взаимодействии с другими веществами они могут претерпевать различные превращения, образуя новые соединения и приводя к изменению свойств и состояния вещества. Это делает молекулярные соединения важными объектами для изучения и понимания механизмов химических реакций.
В заключении, молекулы являются основными строительными блоками вещества и играют решающую роль в его химических свойствах. Молекулярные соединения определяют структуру и поведение вещества, обладая уникальными свойствами и участвуя в химических реакциях. Их изучение имеет важное значение для развития науки и промышленности, а также для составления понятной и связанной картины мира химии.
Влияние молекулярной структуры на физические свойства вещества

Уникальные физические свойства вещества определяются его молекулярной структурой. Каждая молекула состоит из атомов, которые могут быть связаны разными способами, образуя различные типы химических связей. Эти связи определяют физические характеристики вещества, такие как его состояние (твёрдое, жидкое или газообразное) при конкретной температуре и давлении.
Различные физические свойства, такие как плотность, вязкость и точка кипения, зависят от молекулярной структуры. Например, вещества с большим количеством ковалентных связей, имеющих высокую энергию связи, обычно обладают большей плотностью и точкой кипения. С другой стороны, вещества с слабыми межмолекулярными силами, такими как ван-дер-ваальсовы взаимодействия, могут иметь более низкую плотность и точку кипения.
Молекулярная структура также влияет на электрические свойства вещества. Некоторые молекулы могут быть полярными, обладая разделением зарядов внутри молекулы, в результате чего они могут образовывать диполь-дипольные взаимодействия. Другие молекулы могут быть неполярными и не образовывать зарядового разделения, что приводит к слабым межмолекулярным силам. Это различие в электрических свойствах вещества может влиять на его проводимость и реакцию на электромагнитное поле.
Оторному физическому свойству, обусловленному молекулярной структурой, является термическое расширение. Вещества с различной молекулярной структурой могут иметь разные коэффициенты термического расширения в ответ на изменение температуры. Некоторые вещества могут расширяться при нагревании, тогда как другие могут сжиматься. Это явление может приводить к различным практичным последствиям, таким как расширение или сжатие материалов в зависимости от их применения.
Интермолекулярные взаимодействия и их роль в определении характеристик вещества
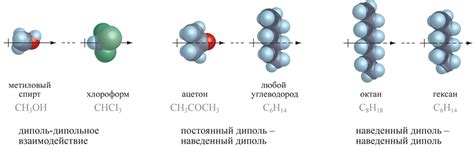
Интермолекулярные силы, возникающие между молекулами, включают в себя такие явления, как ван-дер-ваальсовы силы, диполь-дипольное взаимодействие, а также водородные связи. Такие связи обусловлены различными физическими и химическими свойствами молекул, такими как наличие дипольного момента, электронной плотности, геометрии молекулы и других факторов, которые влияют на закономерности взаимодействия.
Интермолекулярные взаимодействия определяют множество характеристик вещества, таких как температура плавления и кипения, химическая реактивность, плотность, вязкость, теплоемкость и другие физические свойства. Важно отметить, что эти взаимодействия непостоянны и зависят от условий окружающей среды, а также от изменений внутри самой молекулы. Это позволяет нам предсказывать и объяснять поведение веществ в различных условиях и использовать эти знания для создания новых материалов.
Переходы между физическими состояниями вещества и молекулярная структура
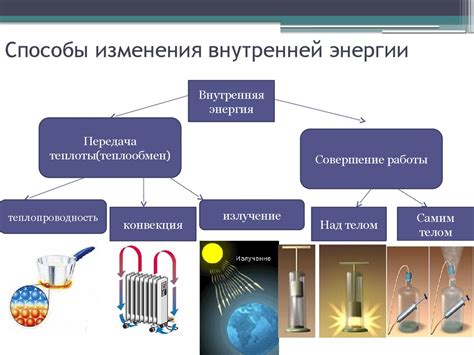
Физическое состояние вещества определяется его молекулярной упаковкой и взаимодействием между молекулами. Вещества могут существовать в трех основных состояниях: твердом, жидком и газообразном. Переходы между этими состояниями происходят при изменении условий окружающей среды.
В твердом состоянии молекулы вещества плотно упакованы и образуют регулярную кристаллическую решетку. В жидком состоянии молекулы находятся в постоянном движении, но сохраняют близкую пространственную организацию. В газообразном состоянии молекулы свободно двигаются и разделены большими промежутками.
Переходы между агрегатными состояниями вещества могут сопровождаться изменением молекулярной структуры. Например, при плавлении твердого вещества молекулы начинают свободно перемещаться, что приводит к нарушению кристаллической решетки. А при испарении жидкости молекулы приобретают большую кинетическую энергию и отрываются от друг друга, образуя газообразное состояние.
Изучение переходов между агрегатными состояниями и молекулярной структурой вещества позволяет лучше понять свойства материи и применять эти знания в различных областях научных и технических дисциплин.
Как устанавливается химический состав вещества?

В химии существует метод определения молекулярного состава вещества, позволяющий узнать из каких молекул оно состоит. Этот метод основан на опыте и имеет надежную основу. Для выяснения молекулярного состава вещества применяются различные подходы, каждый из которых имеет свои особенности и применимость к определенным типам веществ.
Один из основных методов определения молекулярного состава вещества - это анализ химической формулы. Химическая формула выражает соотношение атомов элементов в молекуле вещества. Изучая эту формулу, можно понять, сколько атомов каждого элемента содержится в молекуле и как они соединены между собой. Таким образом, анализ химической формулы позволяет определить, из каких элементов состоит вещество и каким образом они связаны.
Кроме анализа химической формулы, для определения молекулярного состава вещества используются и другие методы. Один из них - спектральный анализ, основанный на изучении взаимодействия вещества с электромагнитным излучением. Путем анализа спектральных данных можно установить наличие определенных элементов или групп функциональных групп в молекуле вещества.
- Анализ химической формулы
- Спектральный анализ
- Физический анализ
Каждый из этих методов имеет свои преимущества и недостатки, и для получения точных результатов часто используется сочетание нескольких методов. Объединенный анализ позволяет установить молекулярный состав вещества с большей надежностью и точностью. Знание молекулярного состава вещества является важной основой для понимания его свойств и использования в различных областях науки и технологий.
Структурные изменения вещества: роль молекул и процессы химических реакций
Когда речь заходит о составе вещества, невозможно не обратить внимание на роль молекул и процессов химических реакций в изменении его структуры. Молекулы, являющиеся основными строительными блоками вещества, играют ключевую роль в его свойствах и поведении. Химические реакции, в свою очередь, представляют собой процессы, в результате которых молекулы изменяют свою структуру, образуя новые соединения и приводя к образованию различных веществ.
| Роль молекул в изменении структуры вещества | Химические реакции и их влияние на структуру вещества |
|---|---|
| Важность молекулярной структуры в определении свойств вещества, таких как температура плавления и кипения, растворимость, химическая активность и многое другое. | Изменения, происходящие в молекулах вещества в результате химических реакций и их влияние на образование новых соединений. |
| Структурные изменения молекул и переходы между различными состояниями вещества (твердом, жидком и газообразном), вызванные внешними условиями и взаимодействиями с другими веществами. | Энергетические и кинетические аспекты химических реакций, включая абсорбцию и выделение тепла, скорость реакции и реакционные механизмы, определяющие изменение структуры вещества. |
Таким образом, изучение взаимосвязи между молекулами и химическими реакциями не только позволяет понять как меняется структура вещества, но и объяснить множество фундаментальных явлений и явиться основой для разработки новых материалов и технологий.
Практическое применение знаний о структуре молекул в науке и технологиях
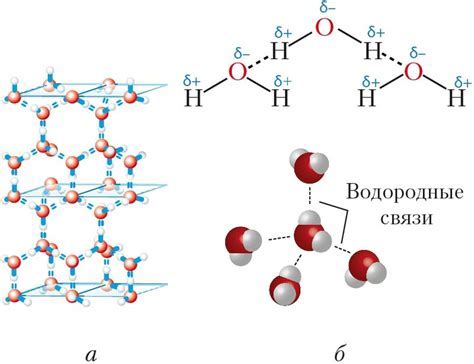
Одним из применений знаний о молекулярной структуре является разработка новых материалов. Используя современные методы исследования, ученые могут определить оптимальную структуру материала для конкретной цели. Например, основываясь на знании о молекулярной структуре, можно создавать материалы с улучшенными механическими свойствами, стойкостью к разрушению или эффективностью проводимости.
Другим важным применением является разработка новых лекарственных препаратов. Зная структуру молекулы белка или целевого органа, ученые могут разработать молекулы-лекарства, которые будут точно взаимодействовать с нужными мишенями в организме. Это позволяет создавать более эффективные и безопасные препараты для лечения различных заболеваний.
Кроме того, знание о молекулярной структуре помогает в разработке новых технологий. Например, в области электроники и компьютерных технологий, понимание взаимодействия молекул и электрического тока позволяет создавать новые материалы для более эффективных и компактных устройств.
Вопрос-ответ

Как можно доказать, что вещество состоит из молекул?
Существует много экспериментальных методов, позволяющих доказать, что вещество состоит из молекул. Один из таких методов - диффузия. Путем наблюдения за движением молекул вещества при распространении аромата или других веществ можно увидеть, что они перемещаются независимо друг от друга, что свидетельствует о молекулярной структуре вещества.
Можно ли визуализировать молекулы вещества?
Да, современные методы научных исследований позволяют визуализировать молекулы вещества. Одним из таких методов является сканирующая туннельная микроскопия. С помощью этой техники можно получить изображение поверхности, на которой находятся молекулы, с высоким разрешением, что дает возможность увидеть их форму и структуру.
Оказывают ли молекулы влияние на свойства вещества?
Да, молекулы оказывают значительное влияние на свойства вещества. Свойства вещества определяются взаимодействием молекул между собой. Например, форма и размер молекул могут влиять на плотность и температуру плавления вещества.
Может ли состояние вещества изменяться при изменении молекулярной структуры?
Да, состояние вещества может изменяться при изменении молекулярной структуры. Например, при сжатии газа молекулы приближаются друг к другу, что может привести к переходу газа в жидкое или твердое состояние. Также, изменение молекулярной структуры может вызвать изменение химических и физических свойств вещества.
Существуют ли вещества, не состоящие из молекул?
Да, существуют вещества, не состоящие из молекул. Примером такого вещества является ионный кристалл, состоящий из ионов, а не молекул. Ионы состоят из атомов, но не объединяются в молекулы, так как не образуют ковалентных связей между собой.