Каждый день мы оказываемся в мире, где атомы и молекулы неустанно двигаются вокруг нас, незаметные для глаза обычного наблюдателя. Эти мельчайшие строительные блоки материи неуклонно совершают танцы, взаимодействуя друг с другом, что создает наш обыденный мир и безграничный космос вокруг нас.
Влияние окружающей среды на скорость перемещения атомов и молекул является фундаментальным процессом в физике и химии. Эти непрерывные движения приводят к возникновению физических и химических изменений, определяющих поведение материала и его способность взаимодействовать с другими элементами. Понимание, какие факторы влияют на скорость движения мельчайших объектов, открывает широкий спектр возможностей для управления и контроля реакциями и свойствами материалов.
За каждым движущимся атомом или молекулой скрывается важная история взаимодействия с окружающей средой. Тепловое движение, электромагнитные поля, давление, концентрация и состав вещества, всё это оказывает воздействие на пути перемещения этих невидимых постройщиков материи. Получив знание о том, как окружающие факторы влияют на скорость движения атомов и молекул, мы расширяем нашу возможность моделировать и предсказывать поведение материалов, от простых ежедневных предметов до сложных химических соединений.
Важность температуры в поддержании движения атомов и молекул

Молекулы и атомы вещества постоянно находятся в случайном движении, причем скорость этого движения зависит от внешних условий, в том числе и от температуры. При повышении температуры молекулы и атомы приобретают большую энергию, что приводит к увеличению их скорости. Данный процесс подчиняется определенной закономерности: с увеличением температуры, скорость движения атомов и молекул увеличивается, а с уменьшением температуры, соответственно, скорость уменьшается.
Высокая температура среды создает условия для плотного взаимодействия атомов и молекул, что приводит к увеличению частоты столкновений. При этом, происходит обмен кинетической энергией между атомами и молекулами, что позволяет им перемещаться и приводит к образованию диффузии и теплопереносу. Одновременно с этим, высокая температура также способствует возникновению более высоких энергетических состояний атомов и молекул, что может вызвать различные химические реакции.
С другой стороны, низкая температура окружающей среды приводит к замедлению движения атомов и молекул, что может привести к их агрегации или конденсации вещества. При низких температурах, атомы и молекулы обладают низкой энергией, что ограничивает их движение и способность к взаимодействию. Поэтому, скорость химических реакций и других физических процессов может существенно снижаться при низких температурах.
- Температура является важным параметром влияния на скорость движения атомов и молекул.
- Повышение температуры увеличивает скорость движения частиц.
- Высокая температура способствует взаимодействию атомов и молекул, обмену энергии и возникновению химических реакций.
- Низкая температура приводит к замедлению движения частиц и ограничивает их способность к взаимодействию и реакциям.
Связь между температурой и кинетической энергией
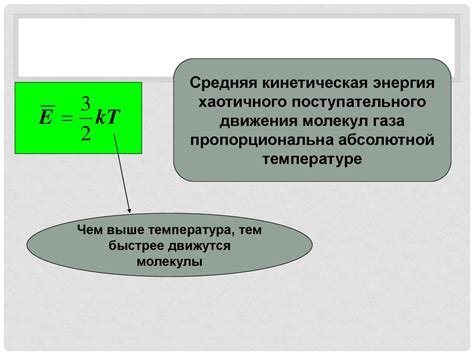
В данном разделе рассмотрим взаимосвязь между величиной температуры и количеством кинетической энергии, присутствующей в системе.
Температура - это мера средней кинетической энергии частиц вещества. Кинетическая энергия, в свою очередь, определяется скоростью и массой частиц. Таким образом, устанавливается непосредственная зависимость между температурой и количеством кинетической энергии.
При повышении температуры частицы вещества начинают двигаться с более высокой скоростью, что приводит к увеличению их кинетической энергии. Обратная ситуация наблюдается при снижении температуры - скорость движения частиц замедляется, и, следовательно, их кинетическая энергия уменьшается.
- Температура является прямым показателем средней энергии, передаваемой молекулами друг другу при столкновениях.
- При повышении температуры, молекулярная дисперсия усиливается, что приводит к увеличению скоростей и количества столкновений между молекулами.
- Тепловое возбуждение вызывает увеличение амплитуды тепловых колебаний молекул и, следовательно, увеличение их скорости.
Таким образом, температура и кинетическая энергия оказывают взаимное влияние друг на друга, определяя движение и поведение молекул и атомов в системе в зависимости от окружающих условий. Более высокая температура соответствует большей кинетической энергии, а следовательно, более активному и интенсивному движению частиц.
Взаимосвязь между давлением и движением частиц
В данном разделе будет исследована важная взаимосвязь между параметром давления и характеристиками движения микрообъектов, таких как молекулы и атомы. Фокус будет сделан на выявление воздействия изменений давления на скорость перемещения частиц в контексте рассмотрения различных частей окружающей среды, вызывающих эти изменения. В результате анализа будут выявлены взаимосвязи между давлением и скоростью движения молекул и атомов.
Основное влияние давления на движение молекул и атомов проявляется в изменении скорости их перемещения. Повышение давления на среду может увеличивать скорость движения частиц, в то время как снижение давления может привести к замедлению перемещения. Из-за этого связи между величиной давления и скоростью молекул и атомов часто выражаются как прямая пропорциональность: с увеличением давления растет скорость движения, а при снижении давления скорость падает.
Давление, которое оказывает воздействие на частицы, является следствием сочетания различных физических и химических факторов окружающей среды. Например, изменения температуры, состава газовой смеси или присутствия других веществ могут вызывать вариации в давлении. В свою очередь, эти изменения давления влияют на движение молекул и атомов, определяя их скорость перемещения.
Распределение движения частиц:

В данном разделе рассматривается влияние контекстуальных условий на движение частиц молекул и атомов. Анализируются особенности распределения скоростей в условиях высокого и низкого давления.
Распределение движения частиц в условиях высокого давления:
Под воздействием высокого давления, движение молекул и атомов происходит с большой энергией и интенсивностью. Это связано с густым окружением, где частицы сталкиваются друг с другом на краткие расстояния. В таких условиях происходит активное перемещение, взаимодействие и перераспределение кинетической энергии.
Высокое давление способствует образованию высоких скоростей частиц. Молекулы и атомы, находясь под огромным давлением, приобретают значительную энергию и подвергаются частым столкновениям. Этот процесс провоцирует равномерное распределение скоростей частиц, где большое количество молекул обладает высокой скоростью, за счет частых и энергичных столкновений.
Распределение движения частиц в условиях низкого давления:
При пониженном давлении, движение молекул и атомов происходит с меньшей интенсивностью. Вокруг каждой частицы образуется большое пространство, поскольку столкновения происходят реже из-за редкого окружения. В таких условиях происходит более свободное движение частиц и перенос энергии между ними.
Низкое давление приводит к распределению скоростей, где можно выделить группы частиц с различными скоростями. Часть молекул и атомов обладает более высокими скоростями, сохраняя свою энергию от предыдущих столкновений, в то время как другая часть имеет меньшие скорости из-за реже происходящих взаимодействий.
Роль концентрации среды в движении микрочастиц
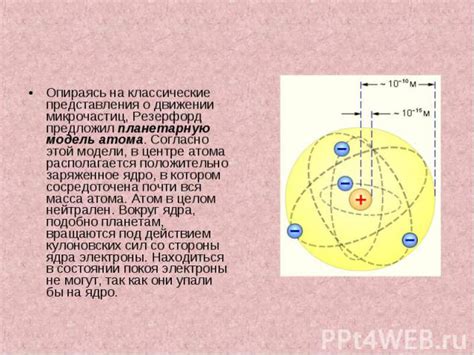
Анализ основных вариабельных компонент движения элементарных частиц вещества позволяет наблюдать значительное влияние концентрации окружающей среды на этот процесс. Концентрация, будучи показателем количества вещества в единице объема, существенно влияет на подвижность молекул и атомов, определяя их скорость и интеракцию друг с другом.
При увеличении концентрации среды происходит увеличение вероятности столкновений между молекулами и атомами, что, в свою очередь, ускоряет их движение. Молекулы и атомы, находясь в более "плотной" среде, испытывают более сильное взаимодействие с другими частицами, что приводит к учащению столкновений и повышению их средней скорости движения.
С другой стороны, снижение концентрации среды приводит к уменьшению вероятности столкновений, в результате чего молекулы и атомы начинают перемещаться с меньшей скоростью. Меньшее количество частиц обуславливает уменьшение количества столкновений и, следовательно, замедление движения молекул и атомов.
Таким образом, концентрация окружающей среды играет значительную роль в движении молекул и атомов, определяя их скорость и способствуя интеракции между частицами вещества. Понимание этой зависимости является важным для более глубокого исследования различных физико-химических процессов и оптимизации условий, в которых они происходят.
| Среда | Концентрация | Скорость движения |
|---|---|---|
| Газ | Высокая | Быстрая |
| Жидкость | Средняя | Умеренная |
| Твердое тело | Низкая | Медленная |
Влияние количества частиц на частоту и силу столкновений
Количество частиц в системе имеет существенное влияние на процессы столкновений, определяющие скорость реакции и формирование новых соединений. Чем больше количество частиц, тем выше вероятность и частота их столкновений, что, в свою очередь, влияет на силу и эффективность этих столкновений.
На молекулярном уровне, увеличение числа частиц приводит к увеличению числа случайных столкновений между ними. Эти столкновения могут приводить к образованию новых химических связей или разрыву существующих. Важно отметить, что частота столкновений пропорциональна числу частиц, поэтому при увеличении их количества, вероятность полезных столкновений, то есть столкновений, приводящих к желаемым реакциям, также увеличивается.
Кроме того, количество частиц оказывает влияние на силу столкновений. Сила столкновения определяется энергией, передаваемой при столкновении между частицами. Большее количество частиц увеличивает вероятность наличия частиц с достаточно большой энергией для прохождения через энергетический барьер реакции. Таким образом, чем больше частиц, тем больше возможностей для больших энергетически заряженных столкновений, способных инициировать сложные химические превращения.
Связь между частотой и силой столкновений
Исследования показывают, что между частотой и силой столкновений существует прямая зависимость. Чем выше частота столкновений в системе, тем больше вероятность сильных и успешных столкновений. Это объясняется тем, что при более высокой частоте столкновений увеличивается шанс наличия частиц с достаточной кинетической энергией для эффективного взаимодействия.
Важно отметить, что частота и сила столкновений также зависят от других факторов, таких как температура и концентрация веществ в системе. Температура влияет на кинетическую энергию частиц и, следовательно, на силу столкновений. Высокая концентрация веществ обеспечивает больше возможностей для столкновений, что также увеличивает частоту и силу столкновений.
Все эти факторы вместе и определяют активность химической системы и ее способность проводить реакции эффективно и быстро. Понимание влияния количества частиц на частоту и силу столкновений позволяет более точно контролировать процессы реакций и оптимизировать их условия в различных научных и промышленных областях.
Влияние размеров частиц на их скорость перемещения

Различия в скорости движения молекул различных размеров при одинаковых условиях

В данном разделе будет исследована зависимость скорости движения молекул от их размеров при одинаковых условиях окружающей среды. Молекулы, являясь основными строительными блоками вещества, обладают различными размерами, что непосредственно влияет на их подвижность.
При одинаковой температуре и давлении, молекулы разных размеров будут иметь разную скорость движения. Молекулы более мелких размеров, такие как атомы, обладают большей подвижностью, чем молекулы больших размеров. Это обусловлено уменьшенной инерцией молекул меньшего размера, что позволяет им быстрее перемещаться в окружающей среде.
| Размер молекулы | Скорость движения |
|---|---|
| Маленький | Высокая |
| Большой | Низкая |
Как показывает таблица, молекулы маленького размера обладают высокой скоростью движения, в то время как молекулы большего размера имеют более низкую скорость. В результате этих различий, молекулы разных размеров взаимодействуют с окружающей средой по-разному.
Определение скорости движения молекул в зависимости от их размеров является важным элементом при изучении различных физических и химических процессов. Дальнейшее исследование данной темы может способствовать более глубокому пониманию влияния размеров молекул и атомов на их поведение в различных реакциях и процессах.
Вопрос-ответ

Какие окружающие факторы могут оказывать влияние на скорость движения молекул и атомов?
Окружающие факторы, которые могут влиять на скорость движения молекул и атомов, включают температуру, давление, концентрацию, химический состав среды, наличие электрического поля и другие факторы.
Каково влияние температуры на скорость движения молекул и атомов?
Повышение температуры обычно приводит к увеличению скорости движения молекул и атомов. Это происходит из-за увеличения количества кинетической энергии частиц, что способствует их быстрому движению в пространстве.
Каково влияние давления на скорость движения молекул и атомов?
Повышение давления обычно приводит к увеличению скорости движения молекул и атомов. При повышенном давлении частицы молекул и атомов сталкиваются друг с другом чаще, что увеличивает их среднюю скорость.
Может ли концентрация влиять на скорость движения молекул и атомов?
Да, концентрация вещества влияет на скорость движения молекул и атомов. При повышенной концентрации частиц молекул и атомов сталкиваются друг с другом чаще, что приводит к увеличению их скорости.
Как влияет химический состав среды на скорость движения молекул и атомов?
Химический состав среды может существенно влиять на скорость движения молекул и атомов. Например, вещества с большей массой могут двигаться медленнее по сравнению с легкими частицами. Также, химические реакции могут приводить к изменению скорости движения частиц в результате образования новых соединений или разрушения старых.