В химической науке существует огромное множество соединений, привлекающих внимание исследователей своей уникальностью и значимостью. Одними из таких соединений являются оксиды, которые представляют собой группу химических соединений, обладающих различными свойствами и используемых в разных сферах человеческой жизни. Однако, среди всего многообразия оксидов выделяются особые, высшая степень окисления которых становится настоящим кульминационным пунктом их взаимодействия с элементами.
Высшая точка окисления в оксидах – это особый уровень, на котором происходит наиболее полное взаимодействие элемента с кислородом. На этой стадии соединение в полной мере раскрывает свои физические и химические свойства, обретая новые качества и способности. Это явление играет немаловажную роль в различных процессах, таких как реакции окисления, синтез новых веществ и даже образование некоторых природных искусственных материалов.
Открытие высшей степени окисления в оксидах стало значимым открытием в химической науке. Благодаря этому открытию, стали возможны новые способы получения важных веществ, а также выработка новых принципов в производстве продуктов массового потребления. Значение высшей степени окисления не может быть недооценено, поскольку она предоставляет уникальные возможности для создания и модификации различных веществ, играющих важную роль в повседневной жизни человека.
Как выявить максимальную окислительную способность оксидов

В данном разделе мы рассмотрим методы, позволяющие определить максимальную способность окисления, обусловленную оксидами различных элементов. Различные химические пробы и эксперименты позволяют сравнивать и классифицировать оксиды по их степени окисления, то есть количеству электронов, которые могут участвовать в окислительно-восстановительных реакциях.
Для начала, можно использовать методы, основанные на анализе химических свойств оксидов. Например, их растворимость в воде или других растворителях может дать представление о их окислительных свойствах. Оксиды, обладающие большей окислительной способностью, будут более растворимыми в различных средах и, следовательно, проявят более активную реакцию с реагентами.
Также можно провести эксперименты, направленные на определение электропроводности оксидов. Электропроводность, связанная с передачей электронов, может помочь определить максимальное количество электронов, которыми обладает оксид. Элементы с более высокими оксидационными состояниями обычно проявляют большую электропроводность.
- Производство газов при нагревании оксидов также может быть использовано для определения максимального окислительного потенциала. Некоторые оксиды распадаются на элементарные газы (например, кислород), что указывает на высокую степень окисления.
- Измерение изменения pH раствора после добавления оксида может дать информацию о его окислительных свойствах. Оксиды с более высокой степенью окисления способны изменять pH раствора более значительно.
- Анализ реакции оксидов с различными металлами и не металлами может также помочь определить их максимальное окислительное состояние. Оксиды, образующие более стабильные соединения с другими элементами, могут иметь более высокую степень окисления.
Вышеуказанные методы исследования позволяют определить высшую степень окисления в оксидах, что является ключевым фактором для понимания их химических и физических свойств, а также их возможных применений в различных областях науки и промышленности.
Роль окисления и оксидации в химии
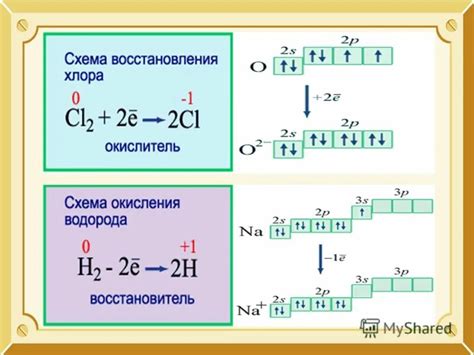
Окисление обычно происходит в результате потери электронов одной или несколькими атомами, а оксидация – это процесс получения электронов атомами других веществ. Такие реакции могут протекать как в атмосфере, так и в живых организмах. Например, окисление соединений серы при сжигании их в воздухе приводит к образованию оксидов серы, а в процессе дыхания в живых организмах происходит окисление органических соединений с образованием оксидов углерода и воды.
В химии оксиды играют важную роль. Они представляют собой химические соединения, в состав которых входит кислород в соединении с другими элементами. Оксиды могут обладать различным оксидационным состоянием, которое определяет уровень окисления элементов в данном соединении. Высшая степень окисления в оксидах характеризует наибольшую потерю электронов со стороны атома связанного элемента и имеет важное значение для понимания свойств и реакционной способности соответствующего соединения.
- Окисление и оксидация - ключевые процессы в химии
- Потеря и получение электронов в реакциях окисления и оксидации
- Примеры окисления в атмосфере и живых организмах
- Оксиды - важные химические соединения
- Определение оксидационного состояния и его значение
Химические свойства оксидов

Кислотные оксиды характеризуются способностью образовывать кислоты при реакции с водой. Они обычно содержат высокую концентрацию кислорода и могут реагировать с основаниями, образуя соли.
Щелочные оксиды, напротив, реагируют с водой, образуя щелочные растворы. Они обладают высокой щелочностью и могут реагировать с кислотами, формируя соли.
Нейтральные оксиды не образуют ни кислоты, ни щелочи при контакте с водой. Они не обладают ни кислотностью, ни щелочностью, и могут реагировать с другими соединениями, образуя разнообразные химические реакции.
- Кислотные оксиды: например, диоксид серы (SO2)
- Щелочные оксиды: например, оксид натрия (Na2O)
- Нейтральные оксиды: например, оксид алюминия (Al2O3)
Химические характеристики оксидов имеют важное значение в промышленности, сельском хозяйстве, медицине и других отраслях. Изучение и понимание этих свойств помогает улучшать производственные процессы, разрабатывать новые материалы и создавать инновационные продукты.
Определение высшей степени окисления с помощью электрохимических методов
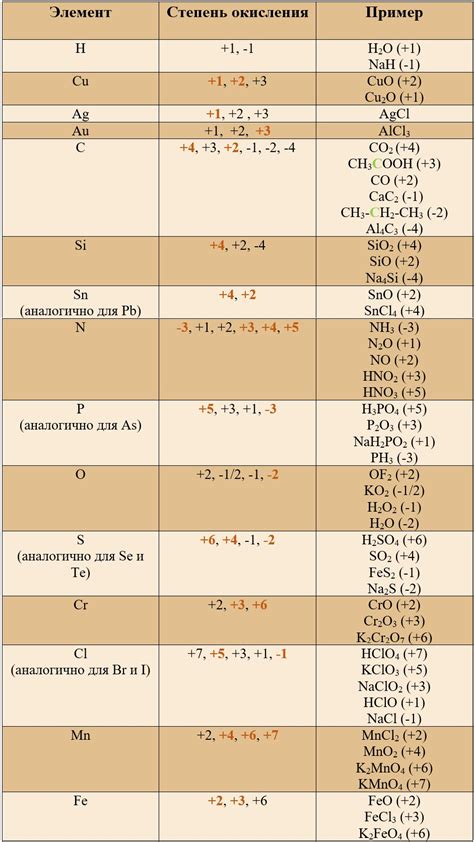
В данном разделе рассматривается возможность определения наибольшей степени окисления в оксидах с использованием электрохимических методов. Это значимая тема, поскольку позволяет установить максимальное значение окисления элемента в соединении, что важно для понимания его химических свойств и использования в различных процессах.
- Электрохимический метод определения высшей степени окисления основан на использовании электролиза и измерении электрического тока, проходящего через реагирующую систему.
- При проведении эксперимента используются электроды, которые вступают в реакцию с окисидом, образуя электролитическую ячейку.
- С помощью контроля тока и определения его изменений, можно установить количество переданных электронов и, следовательно, степень окисления элемента в оксиде.
- Электрохимический метод позволяет обнаружить наибольшую степень окисления, так как при проведении реакции оксида с электродом и последующей регистрации тока, произойдет полное окисление элемента.
- Таким образом, использование электрохимических методов позволяет определить максимальное значение окисления элемента в оксиде, что имеет принципиальное значение при изучении его химических свойств и возможных реакций.
Связь между массой и зарядом: раскрытие высшей степени окисления в оксидах

- Один из ключевых факторов в определении высшей степени окисления связан с массой конкретного атома в оксиде. Большая масса атома может указывать на его способность к окислению и, соответственно, на высшую степень окисления.
- Второй важный аспект - заряд атома. Заряд может быть положительным или отрицательным, и он определяется электронной структурой атома. Чем выше заряд атома, тем выше может быть его степень окисления.
- Соотношение между массой и зарядом является фундаментальной характеристикой вещества, которая может быть использована для определения его высшей степени окисления.
Исходя из этой связи, исследователи могут проводить анализ окислительных реакций на основе массы атомов и их заряда, что помогает не только в определении высшей степени окисления, но и в изучении реакционной способности вещества. Понимание этой связи имеет большое значение для различных областей, включая химическую промышленность, экологию и биохимию.
Роль и важность максимальной окислительной способности в соединениях оксигенированного вещества

- Оксиды с высшей степенью окисления имеют способность к продвинутому окислению других соединений, что отражает их важность во множестве химических процессов, включая синтез и разложение путем передачи электронов.
- Максимальная окислительность в оксидах определяет их электрохимические свойства, такие как потенциал окислительно-восстановительных реакций и электродный потенциал, что применяется в аналитической химии и электрохимических технологиях.
- Высшая степень окисления в оксидах также определяет их физические свойства, включая тепловую и электрическую проводимость, которые находят применение в сфере материаловедения и электроники.
Таким образом, высшая степень окисления в оксидах не только обладает катализирующим эффектом в химических реакциях, но и играет важную роль в удержании и передаче энергии, обуславливая широкое применение оксидов в различных областях науки и промышленности.
Примеры веществ с максимальным окислением и их значимость в промышленности и повседневной жизни

Один из примеров таких соединений – кислород. Он хорошо известен нам как элемент, поддерживающий организмы в живом состоянии и необходимый для существования на планете Земля. Кислород также является важным агентом при проведении различных химических процессов в промышленности: от сжигания горючих веществ до клинического применения в медицине.
Другим примером является пероксид водорода. С его помощью производят стерильность в медицине и косметической промышленности, используют в качестве отбеливающего и антисептического средства. Кроме того, пероксид водорода играет важную роль в процессах окисления вод. Его наличие в окружающей среде определяет важные физико-химические свойства воды, что влияет на ее использование в хозяйственных нуждах.
Еще одним примером является диоксид кремния. Это вещество имеет широкое применение в промышленности, особенно в производстве стекла и керамики. Диоксид кремния также используется в электронике в качестве полупроводника, а в медицине – в составе различных лекарственных препаратов.
Таким образом, примеры веществ с максимальной степенью окисления играют важную роль в разных сферах промышленности и повседневной жизни. Их свойства и способности придают им большую значимость и делают неотъемлемой частью современного мира.
Вопрос-ответ

Что такое высшая степень окисления в оксидах?
Высшая степень окисления в оксидах - это максимальное значение степени окисления атома элемента в соединении с кислородом.
Как определяется высшая степень окисления в оксидах?
Высшая степень окисления в оксидах определяется путем анализа электронной структуры и химических свойств элемента. Обычно она соответствует максимально возможной степени окисления, которую элемент может иметь в соединении с кислородом.
Какое значение имеет высшая степень окисления в оксидах?
Высшая степень окисления в оксидах играет важную роль при определении химических и физических свойств веществ. Она влияет на реактивность вещества, его способность принимать или отдавать электроны, а также на его окислительно-восстановительные свойства.
Какие элементы имеют высшую степень окисления в оксидах?
Высшая степень окисления в оксидах может быть у различных элементов, таких как переходные металлы, неметаллы и полуметаллы. Например, у хрома в хромовом оксиде CrO3 высшая степень окисления равна +6, а у серы в серном оксиде SO3 - +6.